Calcium carbonate và magnesium trong nước cứng là hai tác nhân chính khiến nước sinh hoạt tại nhiều gia đình Việt Nam xuất hiện cặn trắng trong ấm đun, váng mỏng khi pha trà và bọt xà phòng ngày càng ít đi. Hai khoáng chất này tồn tại dưới dạng ion Ca²⁺ và Mg²⁺ hòa tan, hình thành khi nguồn nước ngầm thấm qua các tầng đá vôi và đá dolomite theo chu trình địa chất tự nhiên.
Hiểu rõ bản chất của calcium carbonate và magnesium trong nước cứng là bước đầu tiên để bảo vệ thiết bị gia dụng, tiết kiệm chi phí vận hành và duy trì chất lượng nước sinh hoạt an toàn. Bài viết dưới đây phân tích chi tiết nguồn gốc, cơ chế gây hại, phân loại độ cứng và các phương pháp xử lý hiệu quả được áp dụng phổ biến hiện nay.
I. Mối liên hệ giữa Calcium carbonate, Magnesium và độ cứng của nước
Để xử lý đúng vấn đề nước cứng, trước tiên cần hiểu rõ bản chất hóa học của hai ion quyết định độ cứng: ion canxi (Ca²⁺) và ion magie (Mg²⁺). Hai ion này không xuất hiện ngẫu nhiên, chúng có nguồn gốc địa chất rõ ràng và được đo bằng đơn vị tiêu chuẩn quốc tế.
1.1. Định nghĩa nước cứng theo nồng độ ion Ca²⁺ và Mg²⁺
Nước cứng là loại nước có hàm lượng cation kim loại hóa trị hai. Cụ thể là Ca²⁺ và Mg²⁺ vượt ngưỡng cho phép. Đây là hai ion đặc trưng nhất quyết định độ cứng tổng (Total Hardness) của nguồn nước.
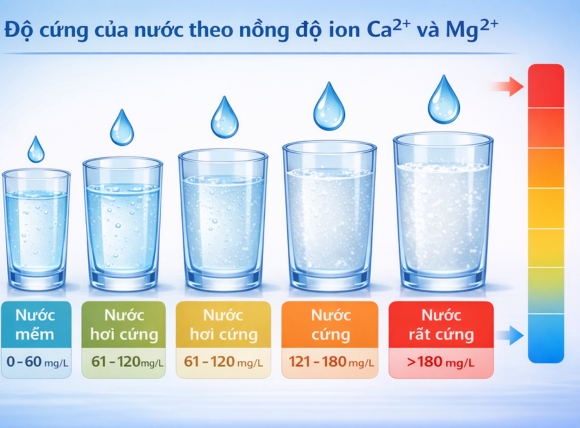
Nước mưa ban đầu gần như không chứa hai ion này. Chúng chỉ xuất hiện sau khi nước thấm qua các tầng địa chất chứa khoáng vật canxi và magie.
1.2. Calcium carbonate, Magnesium có nguồn gốc từ địa chất
Nguồn gốc của calcium carbonate và magnesium trong nước cứng gắn liền với quá trình thấm lọc địa chất qua hàng triệu năm. Khi nước ngầm di chuyển qua các tầng đá vôi (CaCO₃) và đá dolomite CaMg(CO₃)₂, khí CO₂ hòa tan trong nước tạo thành axit carbonic yếu (H₂CO₃).
|
Axit này phản ứng với CaCO₃ theo phương trình: CaCO₃ + CO₂ + H₂O → Ca(HCO₃)₂ (canxi bicarbonate dạng tan trong nước)
|
Tương tự, đá dolomite cung cấp đồng thời cả Ca²⁺ lẫn Mg²⁺ vào nguồn nước ngầm. Đây là lý do vì sao các vùng có nền địa chất đá vôi hoặc đá trầm tích thường ghi nhận độ cứng nước cao hơn so với vùng đá granite hoặc đá biến chất.

Các khoáng vật nguồn gốc điển hình:
- Đá vôi (limestone CaCO₃): Nguồn cung cấp Ca²⁺ chủ yếu.
- Đá dolomite (CaMg(CO₃)₂): Cung cấp đồng thời Ca²⁺ và Mg²⁺.
- Thạch cao (CaSO₄): Nguồn Ca²⁺ tạo nên độ cứng vĩnh cửu.
- Khoáng serpentine: Nguồn Mg²⁺ bổ sung trong một số tầng địa chất.
1.3. Đơn vị đo độ cứng phổ biến (mg/L) tính theo CaCO₃
Độ cứng của nước không đo trực tiếp từng ion riêng lẻ, mà được quy đổi về đương lượng CaCO₃ để thống nhất tiêu chuẩn so sánh. Đơn vị phổ biến nhất tại Việt Nam và quốc tế là mg/L CaCO₃ (tương đương ppm CaCO₃). Ngoài ra còn có các đơn vị:
- °dH (German degree): 1°dH = 17,8 mg/L CaCO₃.
- °f (French degree): 1°f = 10 mg/L CaCO₃.
- GPG (grains per gallon): 1 GPG = 17,1 mg/L CaCO₃.
Tại Việt Nam, đơn vị mg/L CaCO₃ được sử dụng trong các văn bản kỹ thuật và quy chuẩn quốc gia.
II. Hàm lượng Calcium carbonate trong nước cứng theo tiêu chuẩn
Không phải mọi nguồn nước có chứa Ca²⁺ và Mg²⁺ đều được gọi là nước cứng. Việc phân loại phụ thuộc vào ngưỡng nồng độ được xác định bởi các tổ chức tiêu chuẩn quốc tế và quốc gia. Phần này cung cấp khung tham chiếu kỹ thuật để đánh giá mức độ cứng của từng nguồn nước cụ thể.
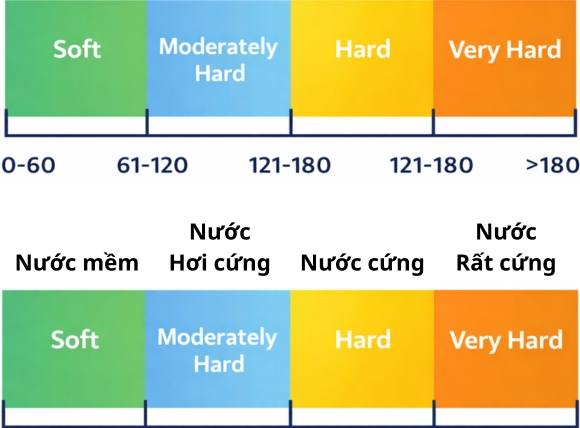
2.1. Bảng phân loại mức độ cứng theo WQA/USGS
Hiệp hội Chất lượng Nước Hoa Kỳ (WQA) và Cơ quan Khảo sát Địa chất Mỹ (USGS) phân loại độ cứng nước theo bốn mức như sau:
|
Phân loại
|
Hàm lượng CaCO₃
(mg/L)
|
Đặc điểm nhận biết
|
|
Nước mềm
|
0 - 60
|
Không có cặn, bọt xà phòng tốt
|
|
Nước cứng vừa
|
61 - 120
|
Bắt đầu xuất hiện cặn nhẹ
|
|
Nước cứng
|
121 - 180
|
Cặn rõ rệt, xà phòng giảm bọt
|
|
Nước rất cứng
|
> 180
|
Cặn dày, vị lạ, thiết bị bị ảnh hưởng
|
Bảng phân loại này là cơ sở kỹ thuật để lựa chọn phương pháp xử lý phù hợp với từng nguồn nước.
2.2. Quy chuẩn Bộ Y tế Việt Nam (QCVN 01-1:2018/BYT) về giới hạn độ cứng trong nước
Theo QCVN 01-1:2018/BYT của Bộ Y tế Việt Nam, giới hạn tối đa độ cứng trong nước ăn uống là 300 mg/L tính theo CaCO₃. Đây là ngưỡng bắt buộc áp dụng cho nước cấp sinh hoạt. Các nguồn nước vượt ngưỡng này cần được xử lý trước khi đưa vào sử dụng cho mục đích ăn uống.

Quy chuẩn này áp dụng đồng thời với các chỉ tiêu khác như pH, TDS, hàm lượng sắt, mangan. Chúng tạo thành bộ tiêu chí đánh giá chất lượng nước toàn diện.
2.3. Ngưỡng >300 mg/L CaCO₃ được xác định là nước rất cứng
Khi hàm lượng CaCO₃ vượt 300 mg/L, nguồn nước được xếp vào nhóm nước rất cứng theo các tài liệu kỹ thuật tham khảo.
Ngưỡng >300 mg/L CaCO₃ được xác định là nước rất cứng
Ở mức này:
- Cặn trắng hình thành nhanh và dày hơn trên bề mặt thiết bị nhiệt.
- Vị nước thay đổi rõ rệt, đặc biệt khi Mg²⁺ chiếm tỷ lệ cao.
- Hiệu suất tẩy rửa của xà phòng và chất tẩy rửa giảm đáng kể.
- Chi phí bảo trì thiết bị tăng theo thời gian sử dụng.
III. Calcium carbonate và Magnesium gây ra cặn trắng khi đun sôi nước
Cặn trắng xuất hiện sau mỗi lần đun sôi là biểu hiện trực quan nhất của nước cứng. Tuy nhiên, không phải ai cũng hiểu rõ cơ chế hóa học đằng sau hiện tượng này. Phần dưới đây phân tích từng phản ứng và quá trình hình thành cặn theo trình tự kỹ thuật.
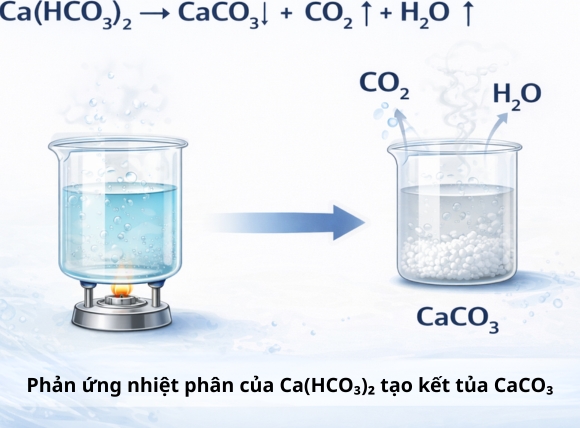
3.1. Phản ứng nhiệt phân của Ca(HCO₃)₂ tạo kết tủa CaCO₃
Canxi bicarbonate Ca(HCO₃)₂ là dạng tồn tại hòa tan của canxi trong nước cứng tạm thời. Khi nhiệt độ tăng lên (thường từ 60°C trở lên), hợp chất này bị phân hủy nhiệt theo phương trình:
|
Ca(HCO₃)₂ →(t°) CaCO₃↓ + H₂O + CO₂↑
|

Kết quả: CaCO₃ kết tủa dưới dạng bột trắng mịn, bám chặt vào đáy ấm, thành bình và thanh nhiệt. Đây chính là lớp cặn vôi trắng (Limescale) mà người dùng quan sát được sau mỗi chu kỳ đun nước.
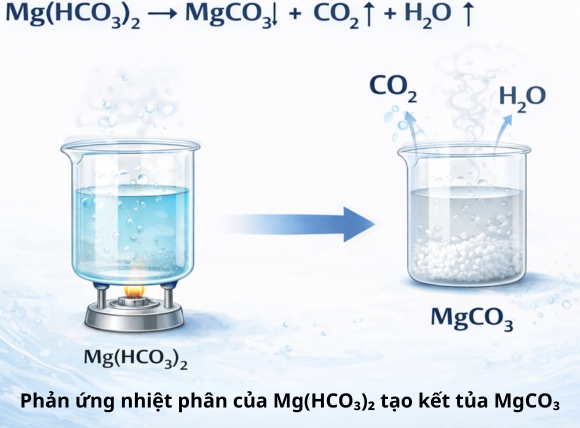
3.2. Phản ứng nhiệt phân của Mg(HCO₃)₂ tạo kết tủa MgCO₃
Tương tự canxi, magie bicarbonate Mg(HCO₃)₂ cũng phân hủy khi đun nóng: Mg(HCO₃)₂ →(t°) MgCO₃↓ + H₂O + CO₂↑.
Điểm khác biệt: MgCO₃ có độ tan cao hơn CaCO₃ ở cùng nhiệt độ, nên lượng kết tủa magie thường ít hơn. Tuy nhiên, ở nhiệt độ cao hơn, Mg²⁺ có thể tạo Mg(OH)₂, một kết tủa trắng khó tan hơn: MgCO₃ + H₂O →(t° cao) Mg(OH)₂↓ + CO₂↑
Hai phản ứng này xảy ra đồng thời trong cùng một ấm đun, tạo ra hỗn hợp cặn CaCO₃ và MgCO₃/Mg(OH)₂ bám trên bề mặt kim loại.
3.3. Cơ chế hình thành lớp cáu cặn (limescale) bám trên thanh nhiệt và đáy ấm đun
Lớp cáu cặn không hình thành ngay lập tức sau một lần đun. Đây là quá trình tích lũy theo chu kỳ với cơ chế như sau:
- Chu kỳ đầu: CaCO₃ và MgCO₃ kết tủa ở dạng hạt mịn lơ lửng trong nước.
- Lắng đọng: Các hạt này lắng xuống đáy hoặc bám vào bề mặt kim loại có nhiệt độ cao nhất (thanh điện trở).
- Thiêu kết: Dưới tác động nhiệt liên tục, lớp cặn cứng lại thành vỏ khoáng dày đặc.
- Cách nhiệt: Lớp cặn dày 1mm có thể làm giảm hiệu suất truyền nhiệt đáng kể, buộc thiết bị tiêu thụ thêm điện năng để đạt cùng nhiệt độ.
IV. Phân biệt độ cứng cacbonat và độ cứng phi cacbonat trong nước cứng
Không phải mọi loại nước cứng đều xử lý được bằng cách đun sôi. Sự khác biệt nằm ở thành phần muối hòa tan tạo nên độ cứng. Phân biệt đúng hai loại độ cứng này là điều kiện tiên quyết để chọn phương pháp xử lý phù hợp, tránh lãng phí chi phí vào giải pháp không hiệu quả.
4.1. Độ cứng cacbonat (nước cứng tạm thời) do Ca(HCO₃)₂ và Mg(HCO₃)₂
Độ cứng cacbonat còn gọi là độ cứng tạm thời, hình thành do sự có mặt của:
- Canxi bicarbonate: Ca(HCO₃)₂
- Magie bicarbonate: Mg(HCO₃)₂

Đặc điểm kỹ thuật quan trọng: loại độ cứng này có thể loại bỏ hoàn toàn bằng cách đun sôi, vì nhiệt phân hủy bicarbonate thành carbonate không tan và CO₂ bay ra ngoài. Đây là phương pháp xử lý đơn giản nhất, không cần hóa chất hay thiết bị chuyên dụng. Phù hợp cho nước sinh hoạt gia đình khi độ cứng không quá cao.
4.2. Độ cứng phi cacbonat (nước cứng vĩnh cửu) do CaSO₄, CaCl₂, MgSO₄, MgCl₂
Độ cứng phi cacbonat còn gọi là độ cứng vĩnh cửu, hình thành từ các muối sulfate và clorua của canxi và magie:
|
Muối
|
Ký hiệu
|
Nguồn gốc phổ biến
|
|
Canxi sulfate
|
CaSO₄
|
Thạch cao trong địa tầng
|
|
Canxi clorua
|
CaCl₂
|
Vùng ven biển, địa chất trầm tích
|
|
Magie sulfate
|
MgSO₄
|
Khoáng epsomite
|
|
Magie clorua
|
MgCl₂
|
Vùng ven biển, mỏ khoáng
|

Các muối này không phân hủy khi đun sôi. Nhiệt độ 100°C không đủ để phá vỡ liên kết sulfate hay clorua. Do đó, nước cứng vĩnh cửu bắt buộc phải xử lý bằng phương pháp hóa học, trao đổi ion hoặc lọc màng.
4.3. Nước cứng toàn phần bao gồm cả hai loại độ cứng trên
Trong thực tế, phần lớn nguồn nước ngầm tại Việt Nam chứa cả hai dạng độ cứng cùng lúc. Vừa có bicarbonate (gây độ cứng tạm thời) vừa có sulfate/clorua (gây độ cứng vĩnh cửu). Tổng hợp hai loại này tạo thành độ cứng toàn phần (Total Hardness).
|
Độ cứng toàn phần = Độ cứng cacbonat + Độ cứng phi cacbonat
|
Đây là chỉ số quan trọng nhất khi đánh giá chất lượng nguồn nước và lựa chọn hệ thống xử lý tổng thể.
V. Tác hại của Calcium carbonate và Magnesium trong nước cứng
Calcium carbonate và magnesium trong nước cứng không chỉ ảnh hưởng đến một khía cạnh duy nhất. Tác động của chúng trải rộng từ thiết bị công nghiệp đến đời sống hằng ngày và sức khỏe người dùng. Mức độ thiệt hại tỷ lệ thuận với hàm lượng Ca²⁺ và Mg²⁺ trong nguồn nước và thời gian sử dụng.
5.1. Đóng cặn CaCO₃ và MgCO₃ trên nồi hơi, ống dẫn, ấm đun
Cặn khoáng hình thành từ CaCO₃ và MgCO₃ là nguyên nhân trực tiếp gây ra các thiệt hại sau:
- Giảm hiệu suất nhiệt: Lớp cặn dày có hệ số dẫn nhiệt thấp hơn kim loại, buộc thiết bị tiêu tốn thêm điện năng để đạt cùng nhiệt độ mục tiêu.
- Tắc nghẽn đường ống: Cặn tích lũy dần theo thời gian thu hẹp tiết diện lòng ống, giảm lưu lượng nước và áp suất hệ thống.
- Rút ngắn tuổi thọ thiết bị: Bình nóng lạnh, máy giặt, ấm điện, nồi hơi công nghiệp đều bị ảnh hưởng khi vận hành liên tục với nước cứng.
- Chi phí bảo trì tăng: Vệ sinh cặn định kỳ hoặc thay thế linh kiện phát sinh chi phí đáng kể trong dài hạn.

5.2. Ion Ca²⁺ và Mg²⁺ phản ứng với xà phòng tạo kết tủa không tan
Khi ion Ca²⁺ và Mg²⁺ tiếp xúc với xà phòng (chứa muối stearate), phản ứng hóa học xảy ra ngay lập tức:
|
2C₁₇H₃₅COONa + Ca²⁺ → (C₁₇H₃₅COO)₂Ca↓ + 2Na⁺
|
Kết quả là canxi stearate, một kết tủa không tan màu trắng đục hình thành thay vì bọt xà phòng. Hệ quả thực tế:
- Lượng xà phòng tiêu thụ tăng do phần lớn bị "trung hòa" bởi ion cứng.
- Quần áo sau giặt có cảm giác thô ráp, cứng và dễ ố vàng theo thời gian.
- Bề mặt tắm không được làm sạch triệt để do màng kết tủa còn bám lại.
- Hiệu quả của chất tẩy rửa công nghiệp giảm, tăng chi phí sản xuất.

5.3. Ảnh hưởng cảm quan của của người dùng
Người dùng tiếp xúc trực tiếp với nước cứng thường nhận thấy các biểu hiện cảm quan rõ ràng:
- Vị đắng hoặc vị lạ: Đặc trưng khi hàm lượng Mg²⁺ vượt ngưỡng, thường trên 125 mg/L.
- Váng mỏng khi pha trà hoặc cà phê: Do kết tủa khoáng hình thành khi tiếp xúc với nước nóng.
- Cặn trắng ở đáy cốc, ấm, vòi nước: Dấu hiệu trực quan dễ nhận biết nhất.
- Cảm giác da khô và tóc xơ sau khi tắm: Do lớp kết tủa canxi bám nhẹ trên bề mặt da và tóc.

5.4. Nguy cơ sỏi thận và các vấn đề tim mạch khi sử dụng nước cứng >300 mg/L lâu dài
Các tài liệu tham khảo đề cập rằng việc sử dụng nước có độ cứng vượt 300 mg/L CaCO₃ trong thời gian dài có thể liên quan đến:
- Nguy cơ hình thành sỏi thận do lượng canxi dư thừa kết tinh trong đường tiết niệu.
- Các vấn đề liên quan đến tim mạch trong một số trường hợp.

Lưu ý: VITEKO khuyến nghị người dùng tham khảo ý kiến bác sĩ hoặc chuyên gia y tế để được tư vấn cụ thể theo tình trạng sức khỏe cá nhân. Thông tin trên không thay thế chẩn đoán y tế chuyên nghiệp.
VI. Phương pháp loại bỏ Calcium carbonate và Magnesium khỏi nguồn nước sinh hoạt
Sau khi xác định rõ loại và mức độ cứng của nguồn nước, bước tiếp theo là lựa chọn phương pháp xử lý phù hợp. Mỗi phương pháp có phạm vi ứng dụng, ưu điểm và giới hạn kỹ thuật riêng biệt. Không có giải pháp "toàn năng", hiệu quả xử lý phụ thuộc trực tiếp vào thành phần và nồng độ ion cứng trong nguồn nước cụ thể.
6.1. Đun sôi
Đun sôi là phương pháp đơn giản nhất, không cần thiết bị hay hóa chất. Tuy nhiên, phạm vi ứng dụng bị giới hạn rõ ràng:
- Hiệu quả: Chỉ xử lý được độ cứng tạm thời (cacbonat), tức Ca(HCO₃)₂ và Mg(HCO₃)₂.
- Không hiệu quả: Hoàn toàn không xử lý được độ cứng vĩnh cửu (phi cacbonat) như CaSO₄, MgSO₄, CaCl₂, MgCl₂.
- Hạn chế thực tế: Không phù hợp cho lượng nước lớn, cặn vôi tích lũy trong ấm đun cần vệ sinh định kỳ.

6.2. Phương pháp hóa học
Xử lý hóa học được ứng dụng chủ yếu trong hệ thống xử lý nước quy mô lớn hoặc công nghiệp. Các hóa chất phổ biến:
- Vôi tôi Ca(OH)₂: Kết tủa Ca²⁺ dưới dạng CaCO₃ và Mg²⁺ dưới dạng Mg(OH)₂, phản ứng Ca²⁺ + Ca(OH)₂ → 2CaCO₃↓ Mg²⁺ + Ca(OH)₂ → Mg(OH)₂↓ + Ca²⁺.
- Soda ash Na₂CO₃: Kết tủa Ca²⁺ theo phản ứng Ca²⁺ + Na₂CO₃ → CaCO₃↓ + 2Na⁺.
- Natri phosphate Na₃PO₄: Kết tủa cả Ca²⁺ và Mg²⁺ đồng thời.

Phương pháp này đòi hỏi kiểm soát liều lượng chính xác và hệ thống lắng lọc sau xử lý.
6.3. Trao đổi ion
Trao đổi ion là phương pháp phổ biến nhất trong hệ thống làm mềm nước dân dụng và công nghiệp nhỏ. Nguyên lý hoạt động là nhựa cationit (hạt resin) mang ion Na⁺ hoặc H⁺ tiếp xúc với nước cứng. Phản ứng trao đổi diễn ra: R-2Na⁺ + Ca²⁺ → R-Ca²⁺ + 2Na⁺ R-2Na⁺ + Mg²⁺ → R-Mg²⁺ + 2Na⁺
Ion Ca²⁺ và Mg²⁺ bị giữ lại trên nhựa, trong khi Na⁺ vô hại được giải phóng vào nước. Kết quả: nước đầu ra có độ cứng giảm đáng kể. Nhựa sau khi bão hòa được tái sinh bằng dung dịch muối NaCl.

Lưu ý kỹ thuật: Nước sau trao đổi ion có hàm lượng Na⁺ tăng. Một số tài liệu y tế đề cập người huyết áp cao nên tham khảo bác sĩ trước khi sử dụng nước qua máy làm mềm trao đổi ion lâu dài.
6.4. Công nghệ lọc màng RO
Lọc màng thẩm thấu ngược (RO - Reverse Osmosis) là phương pháp hiệu quả nhất để loại bỏ ion cứng ở quy mô hộ gia đình và sản xuất nước uống đóng chai.
Nguyên lý: Áp suất cao (thường 3-8 bar) đẩy nước qua màng bán thấm có kích thước lỗ 0,0001 micron, giữ lại hầu hết ion khoáng bao gồm Ca²⁺, Mg²⁺, Na⁺, Cl⁻.
*Bảng hiệu suất loại bỏ ion cứng
|
Chỉ tiêu
|
Tỷ lệ loại bỏ điển hình
|
|
Ca²⁺ (ion canxi)
|
93 - 98%
|
|
Mg²⁺ (ion magie)
|
93 - 98%
|
|
TDS tổng
|
90 - 99%
|
|
Độ cứng tổng
|
> 95%
|

Lưu ý quan trọng: Nước RO sau lọc có độ cứng rất thấp, gần như không còn khoáng chất. Một số quan điểm kỹ thuật khuyến nghị tái khoáng hóa nước RO trước khi sử dụng làm nước uống lâu dài để duy trì lượng Ca²⁺ và Mg²⁺ tối thiểu cần thiết cho cơ thể. Tuy nhiên mức khuyến nghị cụ thể cần tham khảo chuyên gia dinh dưỡng.
6.5. Lắp đặt hệ thống làm mềm nước chuyên dụng tại VITEKO
Đối với các hộ gia đình và doanh nghiệp có nguồn nước cứng ổn định và nhu cầu xử lý liên tục, hệ thống làm mềm nước chuyên dụng là giải pháp bền vững và kinh tế nhất về dài hạn. VITEKO cung cấp các hệ thống xử lý nước cứng được thiết kế phù hợp với:
- Điều kiện nguồn nước tại Việt Nam: Đặc biệt là vùng đồng bằng sông Cửu Long (Nhiễm phèn), vùng đồng bằng sông Hồng (nước ngầm có độ cứng cao) và các khu vực ven biển.
- Quy mô lắp đặt đa dạng: Từ hộ gia đình, chung cư đến nhà máy sản xuất, khu công nghiệp.
- Công nghệ kết hợp: Tích hợp trao đổi ion + lọc thô + lọc tinh để xử lý toàn diện cả độ cứng tạm thời lẫn vĩnh cửu.

Để được tư vấn kỹ thuật và lựa chọn hệ thống phù hợp với chất lượng nguồn nước thực tế, khách hàng có thể liên hệ trực tiếp với đội ngũ kỹ thuật VITEKO để được kiểm tra mẫu nước và đề xuất giải pháp cụ thể.
VII. Kết luận của VITEKO
Calcium carbonate và magnesium trong nước cứng là vấn đề kỹ thuật phổ biến. Tuy nhiên, điều đó thường bị xem nhẹ cho đến khi xuất hiện thiệt hại thực tế trên thiết bị hoặc biến đổi chất lượng nước rõ rệt.

Từ các thông tin tham khảo, có thể thấy Calcium carbonate và magnesium trong nước cứng thường liên quan đến hàm lượng khoáng chất hòa tan trong nguồn nước tự nhiên. Việc tìm hiểu nội dung bài viết này sẽ giúp người dùng hiểu rõ hơn về hiện tượng nước cứng.


Đồng thời, còn hiểu được các vấn đề có thể phát sinh trong hệ thống sử dụng nước. Nếu cần tư vấn thêm về giải pháp xử lý hoặc kiểm soát nước cứng, hãy liên hệ Hotline 091 897 6655 (Miền Nam) / 093 345 5566 (Miền Bắc) để được hỗ trợ nhanh chóng.